Кожа представляет собой фактически большой 2D-орган. Хотя у нее есть и 3D-составляющая – волосяные мешочки (фолликулы) и дермы с различными железками, мышечными и нервными волокнами, с кровеносными и лимфатическими сосудиками. Сама кожа-дерма покрыта тонким эпидермисом, клетки которого активно делятся. Они быстро завершают свой жизненный цикл и, отмирая, дают ороговевающие чешуйки, за что образующие их клетки получили название «кератиноциты» (от греч. «керас» – рог; античные авторы считали, что рога растут из мозга).
Естественно, что на эпидермисе с его богатым поверхностным содержимым живет много микроорганизмов. Как писали, «натуралистами открыты на паразитах паразиты». Действительно, на бактериях и кокках кожи обитают инфицирующие их вирусы. Да не просто вирусы, а «джумбо-фаги» гигантских для них размеров (Джумбо – кличка большого слона в одном из американских цирков, а «джумбо-джетами» называют широкофюзеляжные лайнеры).
По составу кожной микрофлоры можно говорить о возрасте. Так, после рождения на лице доминирует «кути», или накожная бактерия (от cutis – «кожа»), но потом она исчезает, чтобы вернуться вновь в пубертате и стать причиной фурункулов и угрей.
Специалисты Европейской лаборатории молекулярной биологии Института биоинформатики насчитали на коже 622 вида микробов (из них 174 ранее неизвестных), 12 грибков, а также 20 вирусов. Среди микробов встретился и MRSA – золотистый стафилококк, который устойчив к пенициллину. Проблема с этим кокком в том, что он может время от времени вызвать дерматит, воспаление кожной дермы. С другой стороны S. epidermidis широко используется в продуктах по уходу за кожей. В прошлом году одна из австрийских фирм создала вакцину против кутибактерии, вызывающей угри, а трансконтинентальный фармгигант вложился в проект по генетическому редактированию «угреватой» C. acnes.
Генетическое редактирование может использоваться для селективного выключения гена антибиотиковой резистентности, оставляя микроб живым. Он находится в конкурентных отношениях с клостридиумом (C. difficile), который может вызывать кишечные язвы. Язвы, в свою очередь, могут поражать и кожу, особенно после кожных ран. Еще в 2018 году журнал Nature писал, что для борьбы с последними необходимо репрограммировать клетки язвенных краев с помощью переноса генов в составе генома адено-ассоциированых вирусов (AAV). Метод был разработан Институтом Дж. Солка в г. Ла-Джолла (США). Авторы отмечали, что с помощью генетического трансфера можно восстанавливать такую 3D-структуру, как кожа.
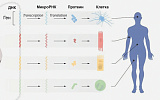
А вот коллеги калифорнийцев из университета в бразильском Сан-Пауло разработали клеточную регенерацию печени. Бразильцы шли по стопам японского лауреата Нобелевской премии С. Яманаки, который выделил квартет генов, введение которых в фибробласты кожи делает их похожими на эмбриональные стволовые клетки. Набор генов включает Oct и Sox, а также Klf и Myc. Достижением бразильцев стало то, что с помощью генного квартета они смогли осуществить омоложение клеток печени непосредственно в организме лабораторных мышей.
Успеху способствовало то, что воздействие осуществлялось всего лишь в течение одного дня. И это резко снизило риск трансформации «юных» клеток. Доказательством этого стало то, что даже через девять месяцев – треть жизни мышей – ни у одной из них не было опухолей. Важность работы подтвердили специалисты Медуниверситета в японском г. Вакаяма. Они отметили: «...факторы Яманаки являются обоюдоострыми: да, они действительно омолодили клетки печени, подстегнув регенерацию органа, и мы рады, что кратковременное их применение дало регенерацию, а не опухолевый рост».
Бразильцы четко показали, что в омоложении важную роль играет также ген Тор, кодирующий фермент топоизомеразу, катализатор изменения топологии («раскручивания») спирали ДНК. Это необходимая начальная стадия в процессе транскрипции (переписывания) генов. Блокирование гена Тор приводило к 40-кратному снижению репрограммирования клеток. Авторы трезво оценивают свой подход, заявляя, что требуется еще огромная работа, чтобы понять молекулярный механизм омоложения и клеточного репрограммирования, прежде чем предлагать клиникам метод терапии, например такого заболевания печени, как жировое перерождение с воспалением.





























комментарии(0)