 Белковый комплекс, который приводит к блокированию синтеза ДНК. Иллюстрации Physorg
Белковый комплекс, который приводит к блокированию синтеза ДНК. Иллюстрации Physorg
Одним из удивительных открытий последнего время стало выявления у бактерий собственной… иммунной системы. Белки и РНК бактериальной иммунной системы сегодня пытаются активно использовать в редактировании генома. Копенгагенский университет обнародовал 3D‑структуру протеинового комплекса сульфобактерии, который можно использовать и для исправления генов человека. Их работа опубликована в журнале Nature Communications.
Самые последние оценки изменений в геноме постулируют наличие до сотни мутаций у новорожденных по сравнению с геномами их родителей. К этому следует добавить 15, которые приобретаются человеком в каждый год его жизни. Двое детей, появившихся в семье с промежутком в 10 лет, различаются на 30 изменений в их геномах. Этот факт установили сотрудники университетов штата Юта в г. Солт‑Лейк‑Cити, Стэнфорда и Колумбийского в Нью‑Йорке. Именно поэтому невозможны пересадки между членами семьи, хотя до этого мать в течение девяти месяцев не отторгала развивающийся плод, который генетически наполовину ей чужероден.

|
|
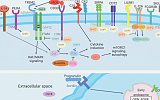
Генетическое редактирование с помощью гид-РНК (голубая). Иллюстрации Physorg |
Старение организма до поры до времени сдерживают стволовые клетки, которые можно получить из фибробластов кожи. Именно в фибробластах синтезируется фибрин, коллаген и другие протеиновые волокна. Не так давно ученые из Колорадского университета научились выделять стволовые клетки у червей. Оказалось, что они локализуются в районе перехода головы в шею. Вполне возможно, что именно это объясняет локализацию эмбрионального «организатора», открытого немцем Хансом Шпеманом. За эту работу немец еще в 1935 году был удостоен Нобелевской премии («за открытие организующих эффектов в эмбриональном развитии»). В своих экспериментах он, например, пересаживал участки кожи от головы на боковую поверхность саламандры, и это приводило к отрастанию пятой лапки.
А четырьмя годами ранее Нобелевской премии удостоили тоже немца Отто Варбурга, открывшего закисление тканей при интенсивной работе или перерождении молочной кислотой (лактатом). Происходит это в результате переключения вырабатывающих клеточную энергию митохондрий с окисления глюкозы на ее бескислородную «обработку».
Сотрудники Института нейронаук в испанском г. Аликанте представили в журнале «Труды АН США» (PNAS) результаты исследования мозговых опухолей (глиобластом). Известно, что мозг защищен от поступления в него различных веществ и инфекций мощным гематоэнцефалическим барьером (ГЭБ). Испанцы выявили роль перицитов в нем. Перициты представляют собой клетки, оплетающие снаружи сосуды. Оказалось, что перициты способствуют росту опухоли. Ученые полагают, что им удалось выявить новую мишень возможного воздействия на развитие внутримозговых новообразований.
В борьбе с ними в последнее время достигнуты определенные успехи, о чем свидетельствует новое лекарство, предложенное молекулярными фармакологами Университета г. Уорвика (Англия). Им помогали коллеги из Университета Сун‑Ятсена в китайском Гуанчжоу‑Кантоне. Исследователи синтезировали молекулярный комплекс, в центр которого поместили иридий. Этот металл известен своей устойчивостью к коррозии. Под действием света комплекс, легко проходящий ГЭБ и оказывающийся в митохондриях опухолевых клеток, в 100 раз эффективнее других веществ лишает опухолевую клетку источника энергии. Эффективность воздействия на опухоли и снижение побочного эффекта достигаются кратковременностью наносекундного светового импульса, не затрагивающего здоровые клетки.
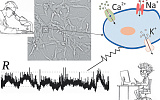
Другой способ доставки лекарств в клетки мозга предложили в Университете Восточной Финляднии в г. Куопио. Он использует белковый транспортер аминокислот, который может переносить через ГЭБ в нейроны и клетки глии молекулы «пролекарств» (prodrugs). Последние активируются при переработке транспортных протеинов в клетках. Вполне возможно, что в скором будущем обе терапии будут дополняться генетическим редактированием.




























комментарии(0)